Calcula el tiempo necesario para que una intensidad de corriente constante de 1.2 A deposite 0.500 g de:
a) ![]() como elemento en un cátodo.
como elemento en un cátodo.
b) ![]() como
como ![]() en un ánodo.
en un ánodo.
c) ![]() como elemento en un cátodo.
como elemento en un cátodo.
Problemas y ejercicios relacionados con los procesos redox, ajuste de reacciones y electroquímica para alumnos de 2º de Bachillerato.
Calcula el tiempo necesario para que una intensidad de corriente constante de 1.2 A deposite 0.500 g de:
a) ![]() como elemento en un cátodo.
como elemento en un cátodo.
b) ![]() como
como ![]() en un ánodo.
en un ánodo.
c) ![]() como elemento en un cátodo.
como elemento en un cátodo.
Un compuesto contiene solamente Fe y O. Una muestra de 0.2729 g de este compuesto se disuelve en 50 mL de disolución ácida concentrada, reduciendo todo el hierro a iones ![]() . La disolución resultante se diluye hasta 100 mL y se valora con una disolución 0.01621 M de
. La disolución resultante se diluye hasta 100 mL y se valora con una disolución 0.01621 M de ![]() . La reacción química, sin ajustar, para la reacción es:
. La reacción química, sin ajustar, para la reacción es:
![]()
En la valoración se gastaron 42.17 mL de disolución de ![]() hasta alcanzar el punto final. ¿Cuál es la fórmula empírica del compuesto?
hasta alcanzar el punto final. ¿Cuál es la fórmula empírica del compuesto?
Masa atómica del Fe = 55.84.
Se desean sintetizar 150 g de anilina a partir de nitrobenceno. Sabiendo que solo el ![]() del nitrobenceno se transforma en anilina en la reacción:
del nitrobenceno se transforma en anilina en la reacción:
![]()
a) Realiza el ajuste de la ecuación por el método ion-electrón.
b) Identifica el agente reductor y el agente oxidante.
c) Calcula las masas de nitrobenceno, NaOH y de ![]() que serán necesarias para obtener la masa deseada de anilina.
que serán necesarias para obtener la masa deseada de anilina.
Datos en 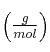 : H = 1 ; C = 12 ; S = 32 ; N = 14 ; O = 16 ; Na = 23.
: H = 1 ; C = 12 ; S = 32 ; N = 14 ; O = 16 ; Na = 23.
Indica si son verdaderas o falsas las siguientes proposiciones, para el caso de una cuba electrolítica:
a) En el cátodo ocurre la oxidación.
b) En el ánodo ocurre la oxidación.
c) Los cationes fluyen hacia el cátodo.
d) En el ánodo los aniones ceden electrones.
Indica si las siguientes afirmaciones son verdaderas o falsas en relación al siguiente proceso:
![]()
a) El estaño se oxida.
b) El ácido nítrico es el agente oxidante.
c) La forma reducida es el dióxido de nitrógeno.
d) El coeficiente del agente reductor es 4.