Dadas las moléculas ![]() ,
, ![]() y
y ![]() :
:
a) Representa sus estructuras de Lewis.
b) Predice la geometría de cada una de ellas según la teoría de repulsión de pares de electrones de la capa de valencia.
c) Indica la polaridad de cada una de las moléculas.
Ejercicios y cuestiones referentes al enlace químico para alumnos de 2.º de Bachillerato.
Dadas las moléculas ![]() ,
, ![]() y
y ![]() :
:
a) Representa sus estructuras de Lewis.
b) Predice la geometría de cada una de ellas según la teoría de repulsión de pares de electrones de la capa de valencia.
c) Indica la polaridad de cada una de las moléculas.
Escribe las estructuras de Lewis de las siguientes especies: $$$ \text{CHF}_3$$$, $$$ \text{NH}_3$$$ y $$$ \text{CH}_3\text{OH}$$$.
Razona si son ciertas o falsas las siguientes afirmaciones:
a) Los orbitales híbridos son moleculares.
b) El número total de orbitales híbridos es igual al número total de orbitales utilizados para su formación.
c) Cuando dos átomos se unen mediante un enlace ![]() y otro
y otro ![]() , diremos que existe un doble enlace.
, diremos que existe un doble enlace.
Indica cuáles de estas sustancias $$$ \text{Cl}_2$$$, CsCl, HBr, CaO, $$$ \text{HNO}_3$$$ y $$$ \text{MgF}_2$$$ son:
a) Covalentes apolares
b) Iónicas
c) Covalentes polares
A partir de los datos de la tabla adjunta, si se forman las moléculas AB, AC, AD y BD:
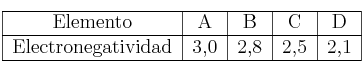
a) Clasifícalas en orden creciente de carácter covalente.
b) ¿Cuál será la molécula más polar? Razona tu respuesta.