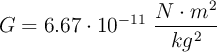De camino a la Luna, los astronautas del Apolo 11 llegaron a punto en el que la fuerza gravitatoria de la Luna era más fuerte que la de la Tierra. Determina la distancia de ese punto al centro de la Tierra.
Datos: ; ; ;
Sabiendo que la estación espacial internacional gira alrededor de la Tierra en una órbita de 386 km de radio, calcula:
a) La velocidad a la que se mueve, expresada en km/h.
b) El tiempo que tarda en completar una órbita.
Datos: ![]() ;
; ![]()
 EjerciciosFyQ
EjerciciosFyQ