Nombra o formula los siguientes alcoholes y fenoles:
a) ![\chemfig{CH_3-CH_2-CH(-[2]C_3H_7)-CH_2-CH_2OH} \chemfig{CH_3-CH_2-CH(-[2]C_3H_7)-CH_2-CH_2OH}](local/cache-TeX/f3f589cecd6a54c7a37607c52f16d2f3.png)
b) ![\chemfig{CH_2(-[2]OH)-CH(-[6]CH_3)-CH(-[2]OH)-C\equiv CH} \chemfig{CH_2(-[2]OH)-CH(-[6]CH_3)-CH(-[2]OH)-C\equiv CH}](local/cache-TeX/0bcab45a5be4d6e50399f9b8e1ddcbe7.png)
c) ![\chemfig{CH_2=CH-CH_2-CH(-[2]OH)-CH=CH-CH_2OH} \chemfig{CH_2=CH-CH_2-CH(-[2]OH)-CH=CH-CH_2OH}](local/cache-TeX/1b65bcc42f9b4c21404f4308d689fb29.png)
d) 2,4,6-triclorofenol
e) 3-isopropilfenol
f) 5-propil-3-heptin-1,6-diol
 EjerciciosFyQ
EjerciciosFyQ
Ejercicios Resueltos, Situaciones de aprendizaje y VÍDEOS de Física y Química para Secundaria y Bachillerato
Nombra o formula los siguientes alcoholes y fenoles:
a) ![\chemfig{CH_3-CH_2-CH(-[2]C_3H_7)-CH_2-CH_2OH} \chemfig{CH_3-CH_2-CH(-[2]C_3H_7)-CH_2-CH_2OH}](local/cache-TeX/f3f589cecd6a54c7a37607c52f16d2f3.png)
b) ![\chemfig{CH_2(-[2]OH)-CH(-[6]CH_3)-CH(-[2]OH)-C\equiv CH} \chemfig{CH_2(-[2]OH)-CH(-[6]CH_3)-CH(-[2]OH)-C\equiv CH}](local/cache-TeX/0bcab45a5be4d6e50399f9b8e1ddcbe7.png)
c) ![\chemfig{CH_2=CH-CH_2-CH(-[2]OH)-CH=CH-CH_2OH} \chemfig{CH_2=CH-CH_2-CH(-[2]OH)-CH=CH-CH_2OH}](local/cache-TeX/1b65bcc42f9b4c21404f4308d689fb29.png)
d) 2,4,6-triclorofenol
e) 3-isopropilfenol
f) 5-propil-3-heptin-1,6-diol
Nombra los siguientes compuestos alicíclicos y aromáticos:
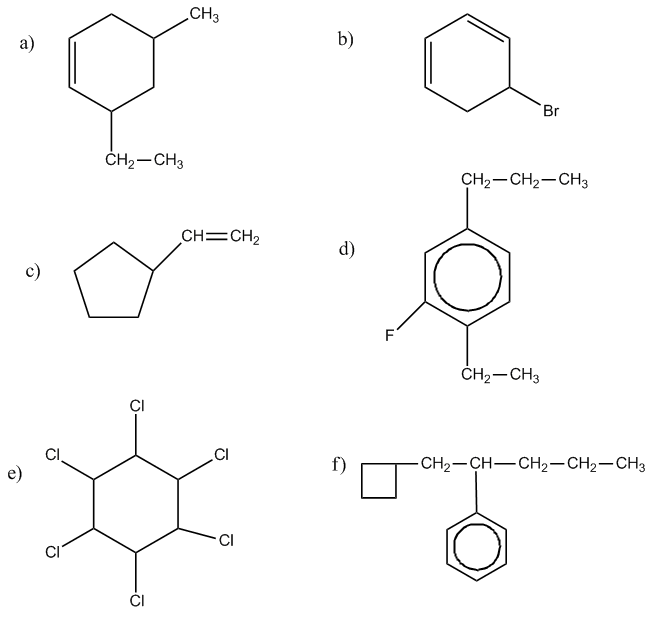
Formula los siguientes compuestos:
a) 1,3-ciclohexadieno
b) 1,6-dimetilciclohexen-3-ino
c) m-butilyodobenceno
d) p-clorotolueno
e) 2,3-dibromopentano
Formula los hidrocarburos insaturados:
a) 2-etilhexa-1,3-dieno
b) hex-1-en-4-ino
c) 4,8-dimetilnona-2,4-dien-6-ino
Formula los alcanos:
a) 3,4-dietil-6-isopropil-2,3,6,7-tetrametilnonano
b) 5-(1,2-dimetilpropil)-8-etil-2,3,3-trimetildecano